【病毒学技术】IgG抗体简介及纯化方式
IgG抗体简介
首先介绍一下我们熟知的免疫球蛋白,一般教科书常提的主要有5种,除了了功能不同外,其主要的却别在于轻链和重链的组成不同,图1所示。对于我们做病毒学实验的小伙伴们来说最熟悉的莫过于初次感染IgM几倍升高,恢复期为IgG诸如此类的了。
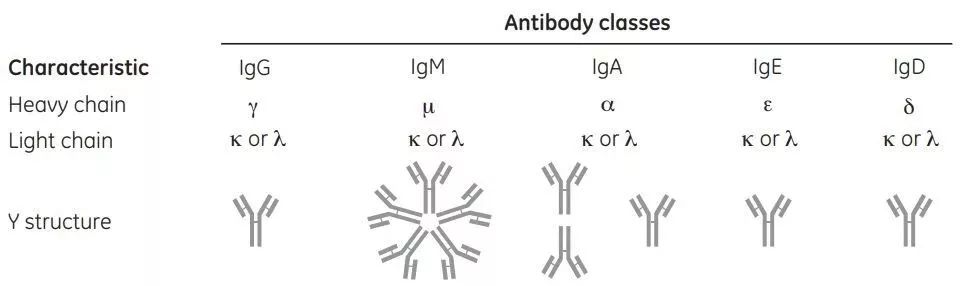
图1:不同免疫球蛋白分子结构示意图
做免疫学的实验中最常碰见的是IgG,就是免疫球蛋白G。其分子的结构见图2所示,IgG作为机体的免疫卫士,主要在机体免疫中起保护作用,对抗大部分的细菌和病毒,IgG是唯一能通过胎盘的免疫球蛋白,IgG能够激活补体系统,参与抗体介导的细胞毒性即ADCC作用,同时参与部分超敏反应。I
gG是由两条重链和两条分子量较小的轻链组成的一个四肽,并且呈现为Y字型的结构,各个链之间由二硫键进行连接,分子量大约为150kDa, IgG 分子是血液中含量很高的一种糖蛋白,在正常人血液中,几乎所有 IgG 的Fc部分都含有至少两个保守的 N- 糖基化位点。
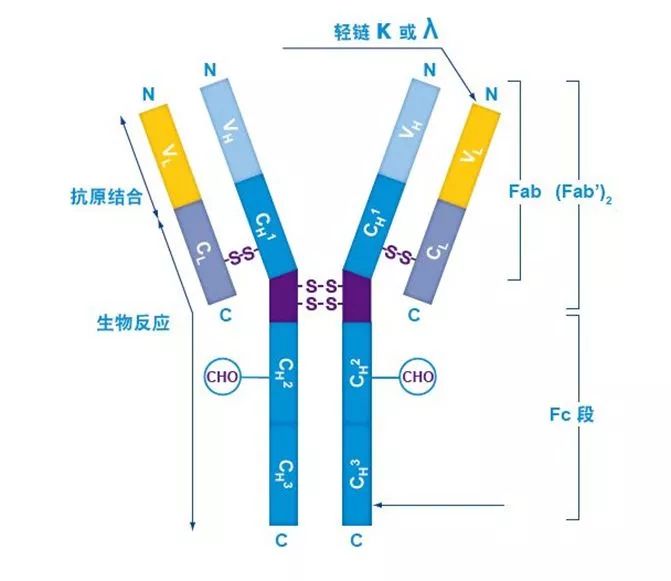
图2:免疫球蛋白G的分子结构模式图
此外,部分抗体的Fab上存在 N- 糖基化位点。人lgG可分为四个亚类,包括IgG1、IgG2、IgG3和IgG4,它们之间的区别是铰链区氨基酸的组成以及重链二硫键的数量和位置的不同。随着研究的不断深入,抗体片段应用也非常广泛,如单链抗体ScFv在抗体药中的应用。

IgG抗体的常见纯化方法
那么如何才能够对IgG进行高效的纯化呢?目前比较成熟的的纯化方法主要有两种,即Protein A和Protein G纯化IgG,那么其原理是什么呢?
1. Protein A
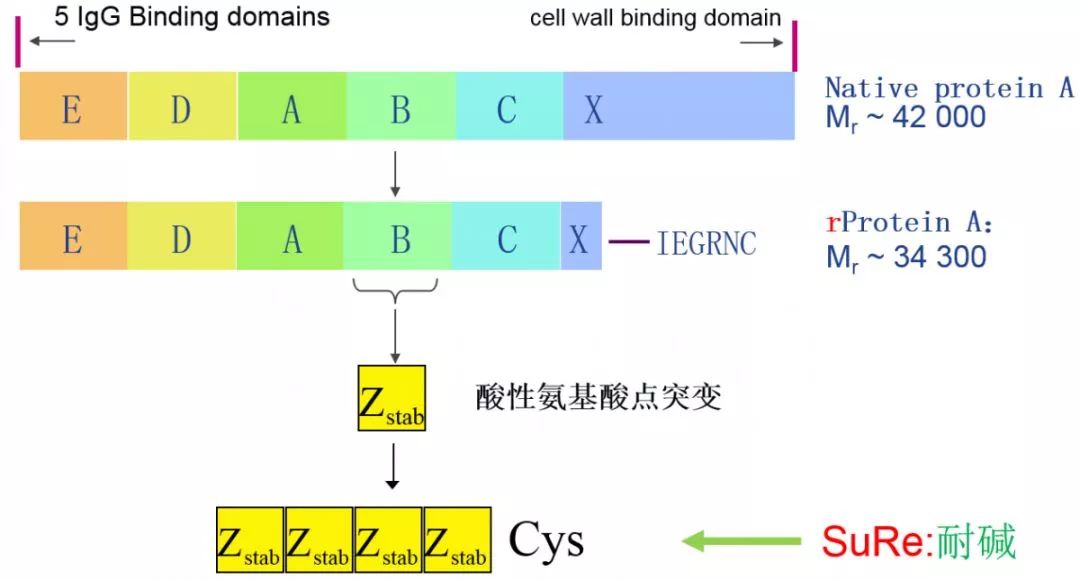
20世纪中期,Jensen发现有一种蛋白可以与人和兔血清抗体广泛结合,该蛋白于1964年首次被称为Protein A。 Protein A是一种金黄色葡萄球菌细胞壁蛋白质,分子量42KD,它能够特异性地结合多种免疫球蛋白的Fc区而与Fab区结合很弱。天然的Protein A有5个IgG结合结构域和未知功能的非Fc结合域,结构示意图如下:
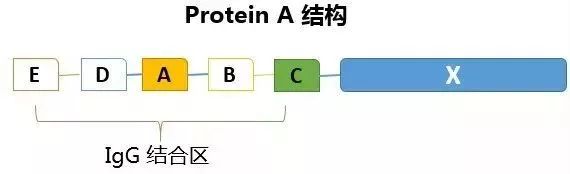
此结构的蛋白A大量结合IgG的同时,其非Fc结合域能结合部分杂蛋白,导致洗脱下来的IgG纯度不够,因此科学家利用基因工程的方法克隆Protein A的基因并进行改造,得到重组蛋白A,其非特异性结合明显降低。下图展示重组蛋白A的偶联方式和载量:
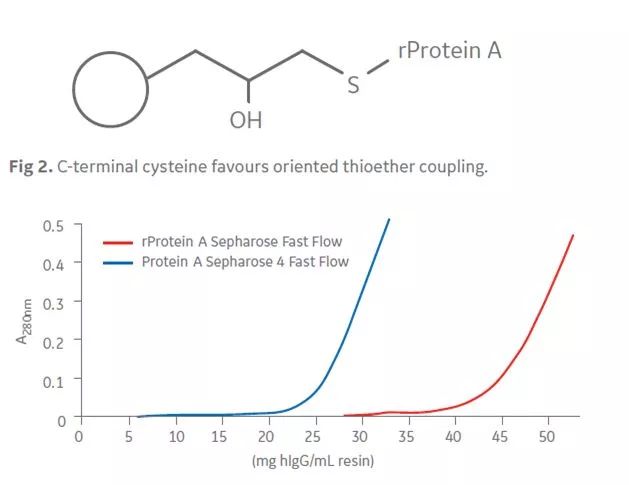
重组蛋白A将蛋白A的结合结构域进行保留,分子量变为35KD,末端经过改造后加上一个C端的半胱氨酸,利用环氧活化的方式单点偶联到琼脂糖上,降低空间位阻的同时提高IgG的结合能力。一步亲和层析后样品纯度可超过90%。重组蛋白A的5个结合结构域中,其中B位点的结合能力更强,因此构建了新的Sure配基,将其中不耐碱的氨基酸进行了改造,因此Sure配基耐碱性更强,且载量更高。
2. Protein G
蛋白G来自于链球菌G族的细胞表面蛋白,是III型Fc受体,分子量为25KD,其通过类似于蛋白A的非免疫机制而结合抗体的Fc段,蛋白G与蛋白A均可结合抗体的Fc段,不同的是,蛋白G还能结合Fab段,且蛋白G可以更广泛的结合更多类型的IgG分子,多克隆IgG分子,同时蛋白G与血清蛋白结合水平低,产物纯度高,且配基脱落更低。抗体基本结构和蛋白A/G的结合位点如下图所示:
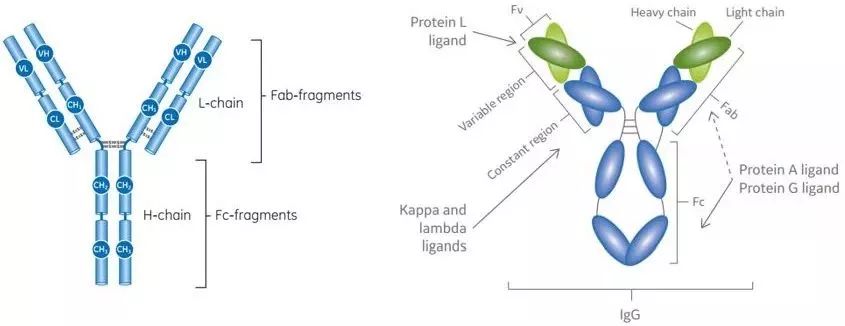
蛋白G可以纯化不能与蛋白A结合的哺乳动物抗体。重组型的蛋白G经改造后已经去除了白蛋白结合位点(血清白蛋白是抗体来源的主要污染物)及细胞表面结合位点,减少了非特异性结合。
3. Protein A 和G亲和力对比
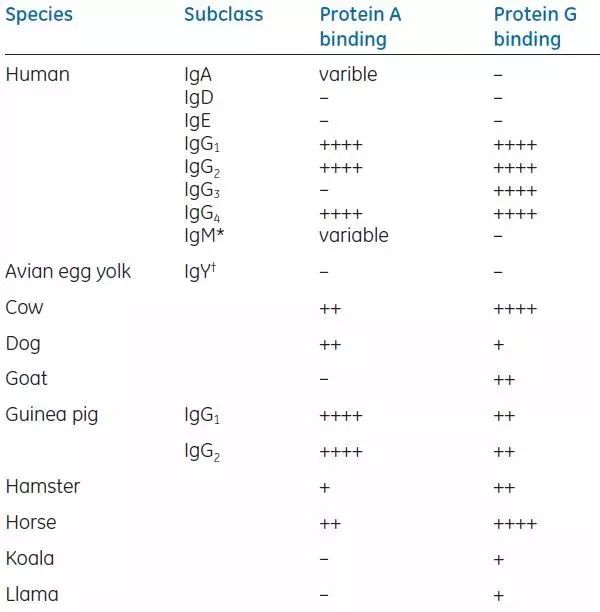
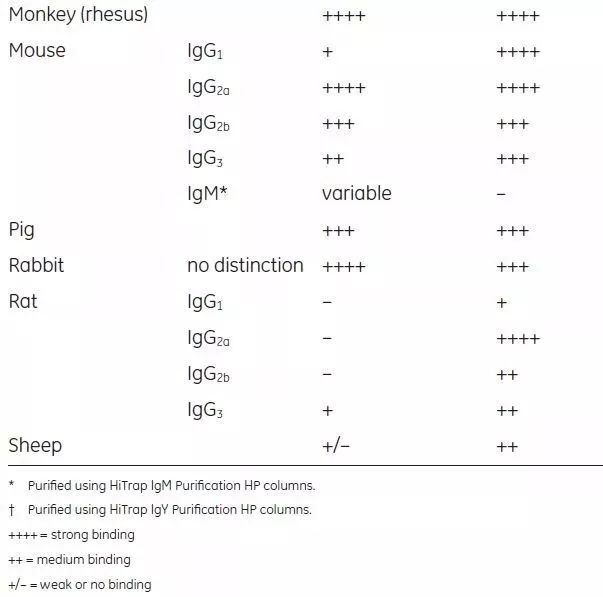
蛋白A和蛋白G对于不同种属和不同亚型的抗体结合能力差异如下表所示,蛋白A对兔来源抗体的亲和力较高,蛋白G对于小鼠等部分哺乳动物抗体的亲和力较高。
现在对于免疫球蛋白及纯化,小伙伴们是否有了更深入的认识呢?继续讨论可点击http://www.virology.com.cn/thread-262919-1-1.html转入中国病毒学论坛继续。
本文来源:摘自“中源生物”微信号
本期编辑:hantavirus
